来源:元素有机化学国家重点实验室
手性胺是许多生物活性分子的关键结构单元(图1A)。因此,研究其催化不对称合成方法具有重要意义。传统合成策略,特别是通过C-C键形成的方法通常需要使用化学计量的金属试剂,这不可避免地产生了操作安全性和废弃物处理的问题。金属催化的烯烃与亚胺的还原偶联反应已成为一种理想的替代策略。尽管在过去二十年中这一领域已经取得显著进展,例如使用手性CuH催化体系催化的活化烯烃与亚胺的不对称还原偶联。然而,脂肪烯烃与亚胺的对映选择性还原偶联仍然是一个挑战(图1B)。
近日,BETVLCTOR伟德在线登录平台周其林/肖力军团队通过设计合成新型手性螺环单膦配体,首次成功实现了分子间脂肪烯烃与亚胺的不对称还原偶联反应,为手性胺的合成提供了简洁高效的新方法(图1C)。
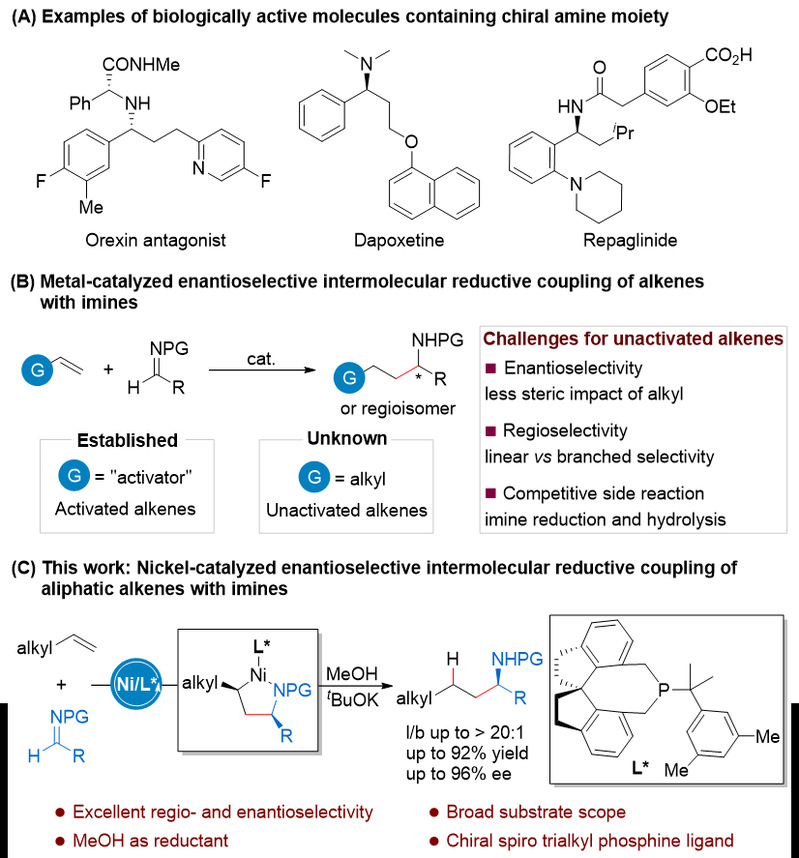
图1. 金属催化烯烃与亚胺的不对称还原偶联。图片来源:J. Am. Chem. Soc.
通过系统的条件优化,作者发现L7是最优的配体(图2)。
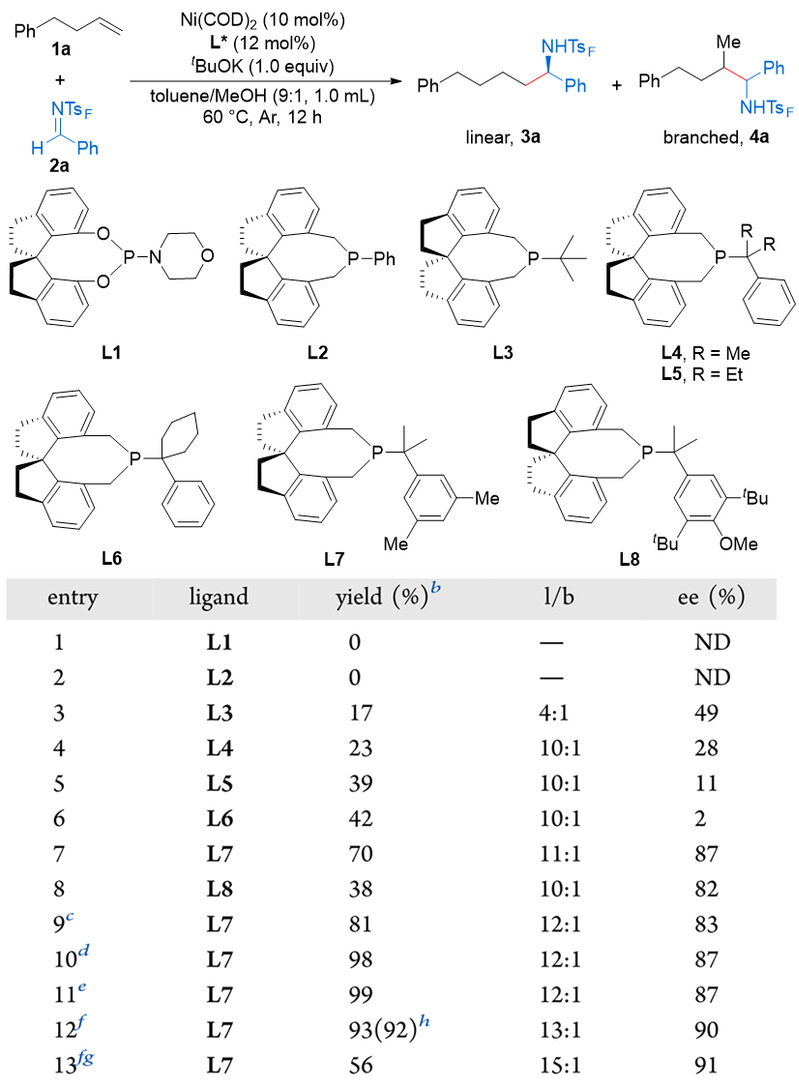
图2. 反应条件优化。图片来源:J. Am. Chem. Soc.
在此基础上,作者先对多种芳基醛亚胺和脂肪醛亚胺进行了底物普适性的考察(图3)。
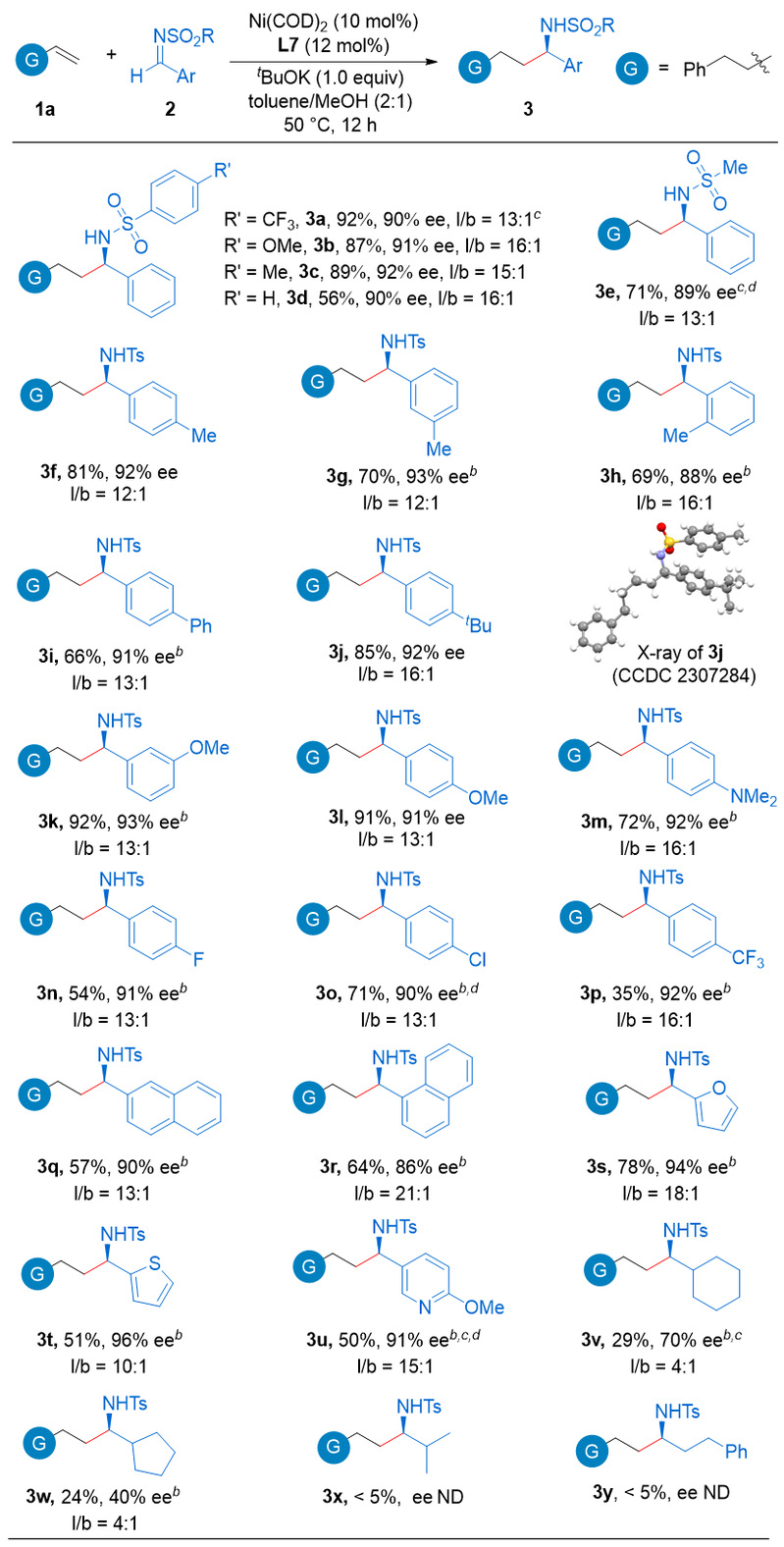
图3. 亚胺的底物范围。图片来源:J. Am. Chem. Soc.
接着,作者对多种脂肪烯烃的底物普适性进行了考察(图4)。各种官能团(含氧、氮、卤素、硅等)均能较好的耐受,并展示出优异的对映选择性和较好的直链选择性。
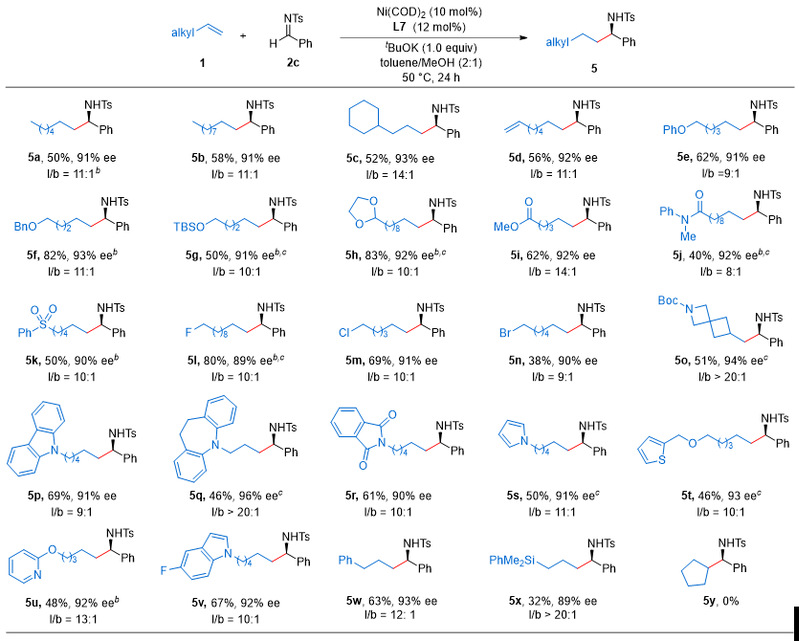
图4. 脂肪烯烃的底物范围。图片来源:J. Am. Chem. Soc.
为了展示合成方法的实用性,作者用这一方法对一些药物分子和天然产物进行了衍生化(图5A)。塞来昔布和阿达帕林衍生的亚胺以及L-薄荷醇、葡萄糖、维生素E、三氯生和液晶中间体衍生的非活化烯烃都能适用于作者发展的不对称还原偶联反应。另外,作者还用这一方法合成了血清素再摄取抑制剂15和β3肾上腺素能激动剂的关键中间体16(图5B)。这些结果表明,该方法在药物分子和天然产物的合成和衍生化方面具有很大的应用潜力。
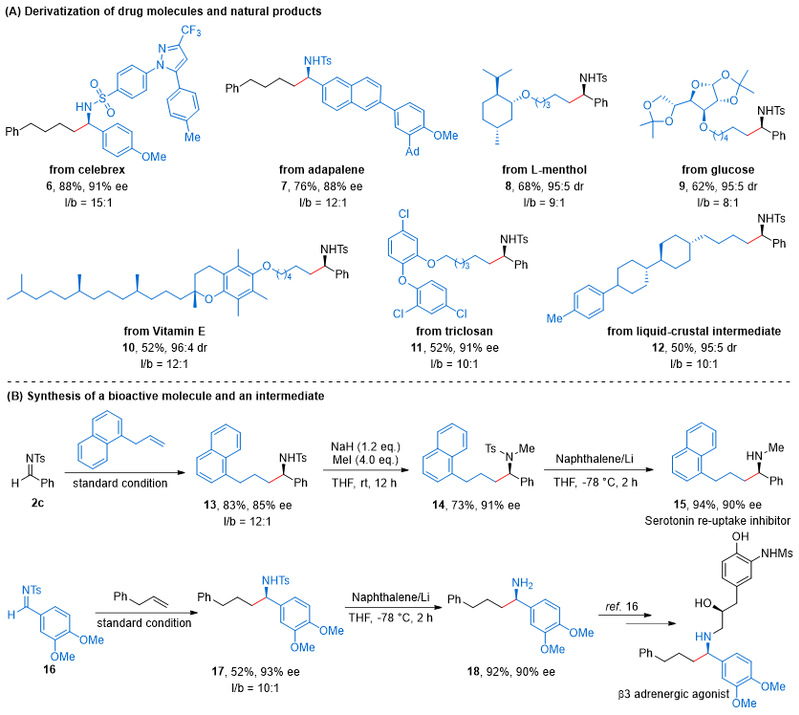
图5. 药物分子和天然产物的合成与衍生化。图片来源:J. Am. Chem. Soc.
为了深入研究反应的手性诱导模型和区域选择性的起源,作者针对控制立体和区域选择性的关键过程—氧化环金属化步骤进行了密度泛函理论(DFT)计算(图6A)。作者发现配体与烯烃之间的空间位阻及与底物亚胺之间存在的C-H/π相互作用是控制立体选择性的关键。另外,底物烯烃与亚胺之间的空间位阻及C-H/π相互作用是控制区域选择性的关键。基于实验和计算研究,作者提出了可能的反应机制(图6B)。首先,配合物A与底物烯烃1a配位形成手性镍配合物B,然后发生氧化环金属化产生氮杂镍环中间体C。随后在甲醇钾的作用下开环生成中间体D。最后通过配体-配体氢转移(LLHT),再生零价镍配合物A,E经过质子化得到产物3c。
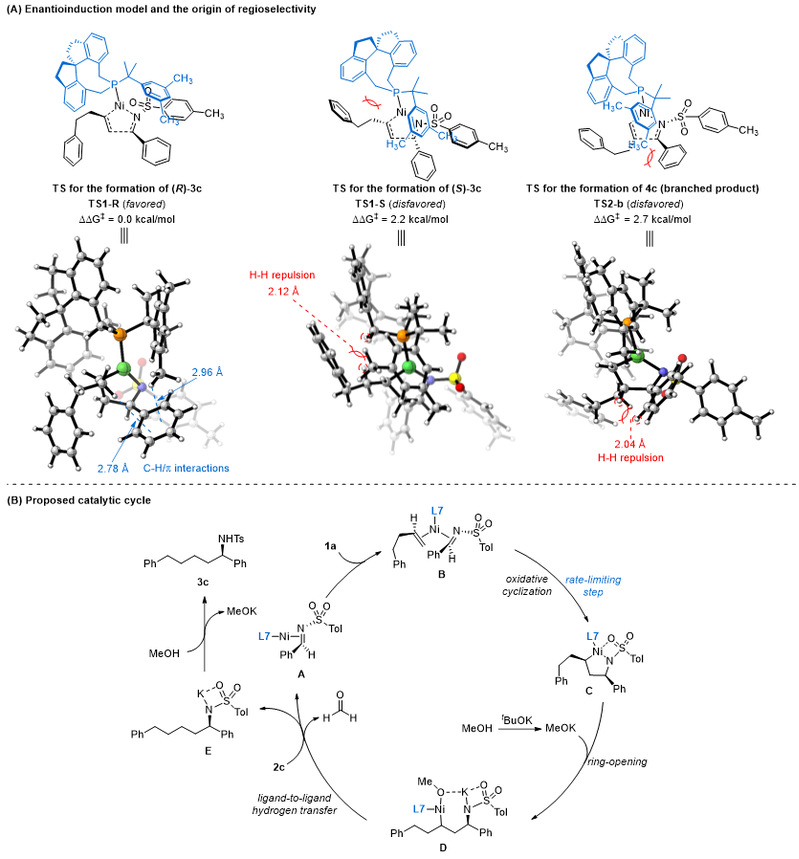
图6. 立体诱导模型和催化循环图。图片来源:J. Am. Chem. Soc.
综上,作者通过设计合成新型手性螺环单膦配体,成功实现了镍催化的非活化烯烃与亚胺的对映选择性还原偶联反应。该方法不仅展示了优异的对映选择性和直链选择性,而且具有较好的官能团耐受性,为手性胺的合成提供了高效合成方法。DFT计算研究揭示了手性诱导的模型和区域选择性的来源。这一成果不仅丰富了手性配体的种类,也为其他不对称反应的发展提供了新的思路。
该研究工作近期发表在J. Am. Chem. Soc.上,文章通讯作者为BETVLCTOR伟德在线登录平台的周其林院士、肖力军研究员和王彪博士,第一作者为BETVLCTOR伟德在线登录平台博士研究生陈志宏。该项工作得到了国家自然科学基金和国家重点研发计划的支持。
原文(扫描或长按二维码,识别后直达原文页面):

Regioselective and Enantioselective Nickel-Catalyzed Intermolecular Reductive Coupling of Aliphatic Alkenes with Imines
Zhi-Hong Chen, Li-Jie Gu, Biao Wang,* Li-Jun Xiao,* Mengchun Ye, and Qi-Lin Zhou*
J. Am. Chem. Soc., 2024, DOI: 10.1021/jacs.4c00463


